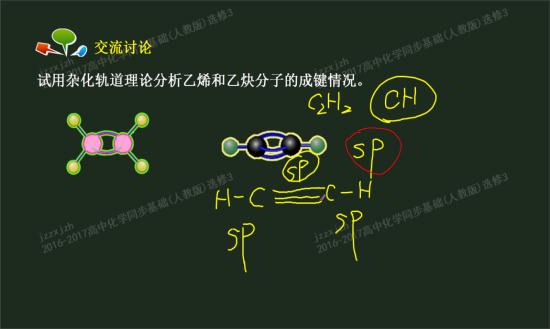
为什么乙炔分子中C原子是sp杂化?CH中_高二
550x329 - 18KB - JPEG

麻烦解释下聚乙炔分子中所有碳原子为什么不可
694x410 - 95KB - JPEG

为测定乙炔的相对分子质量,某小组利用下图所
434x168 - 11KB - JPEG

为测定乙炔的相对分子质量.某小组利用如图所
392x175 - 10KB - JPEG

为测定乙炔的相对分子质量.某小组利用如图所
379x176 - 20KB - PNG

张家口爆燃事故直接原因:氯乙烯气柜泄漏!23死
500x214 - 10KB - JPEG

根据如图回答问题:(1)写出图中有标号的仪器名
327x211 - 13KB - PNG

沸点比氯乙烷高.比乙醇低 ④易溶于水的原因是
278x143 - 7KB - JPEG

为何科学家寻找外星生命要是碳基生命?硼基、
500x455 - 34KB - JPEG

的是( ) A.元素性质呈周期性变化的根本原因是
214x188 - 12KB - PNG

沸点比氯乙烷高.比乙醇低 ④易溶于水的原因是
210x114 - 4KB - JPEG

的广泛存在是造成有机物种类繁多的唯一原因B
221x124 - 29KB - PNG

如图1是实验室制取气体的一些装置.据图回答有
309x112 - 3KB - PNG

0.1mol.L的碳酸钠溶液.碱性更强的是 .其原因是
276x151 - 6KB - JPEG
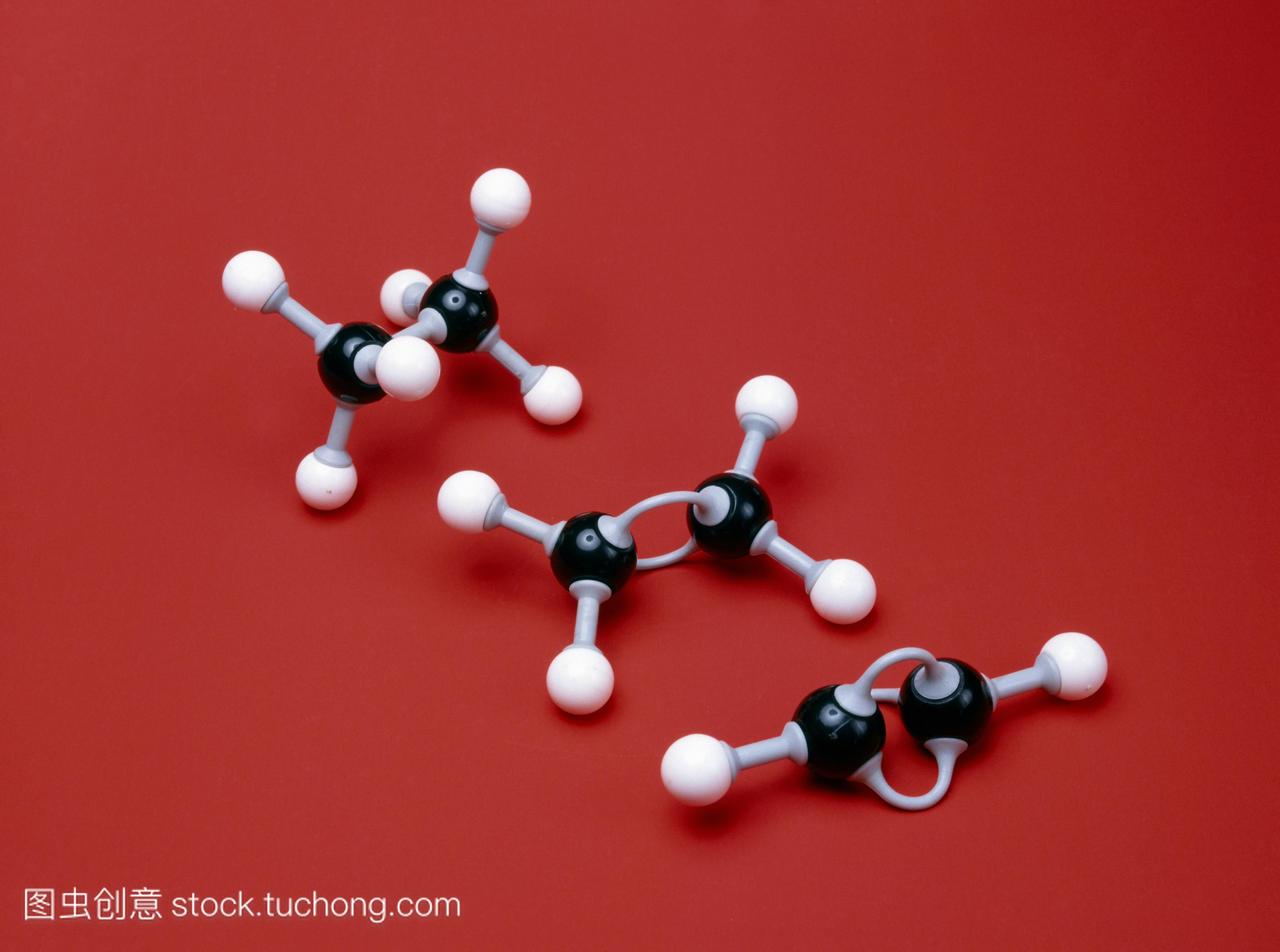
乙烷,乙烯和乙炔分子。乙烷的分子模型c2h6,上
1280x952 - 138KB - JPEG
这个涉及原子轨道和分子轨道的问题。氢原子只有1个电子基态下处于能量最低1s轨道。而碳原子有6个电子,两个位于1s轨道,不参与成键,4个位于第二层上。当形成乙炔时,4个位于最外层的原子轨道发生杂化,即一个s轨道和一个p轨道杂化成两个sp轨道,另外的两个2p轨道保持不变。这样在形成乙炔时,碳原子的其中一个sp轨道与氢原子的1s轨道头碰头重叠,形成 C-Hσ键,另一个sp轨道则与另个碳原子的sp轨道头碰头重叠形成C-Cσ键。碳原子剩下的两个p轨道则肩并肩重叠形成两个C-Cπ键。所以乙炔中有 3个σ键与2个π键,具体说就是两个C-Hσ键,一个C-Cσ键和两个C-Cπ键。希望你能理解原子轨道,杂化,原子轨道的组合和分子轨道。
在乙炔分子中有3个σ键、两个π键,它们分别是( ) A.sp杂化轨道形成σ键、未杂化的两个2p轨道形成两个π键,且互相垂直 B.sp杂化轨道形成σ键、未杂化的两个2p轨道形成两
乙炔是2个σ键,2个π键,σ键全为C-H间的,π键是C-C间的
欢迎来到乐乐题库,查看习题“在乙炔分子中有3个σ键、两个π键,它们分别是( )”的答案、考点梳理,并查找与习题“在乙炔分子中有3个σ键、两个π键,它们分别是( )”相似的
因为这三个分别是单键,双键,叁键,单键由s电子云重叠而成,双键其中有p电子云重叠的部分,电子云密度逐渐加大,键越稳定,键能越短,键越短。
在乙炔分子中有3个σ键、两个π键,它们分别是A.sp杂化轨道形成σ键、未杂化的两个2p轨道形成两个π键,且互相垂直B.sp杂化轨道形成σ键、未杂化的两个2p轨道
2.乙炔分子中有3个σ键.两个π键.它们分别是( )A.C-H之间是sp形成的σ键.C-C之间全是未参加杂化的2p轨道形成的π键B.C-C之间是sp形成的σ键.C-H之间是未参加杂化的2
因为这三个分别是单键,双键,叁键,单键由s电子云重叠而成,双键其中有p电子云重叠的部分,电子云密度逐渐加大,键越稳定,键能越短,键越短. 作业帮用户 2016-11-22 其他类似问
碳原子形成乙炔时,一个2s轨道和一个2p轨道杂化成两个sp轨道,另外的两个2p轨道保持不变,其中一个sp轨道与氢原子的1s轨道头碰头重叠形成C-H σ键,另一个sp轨道则与另个
在乙炔分子中有3个σ键、两个π键,它们分别是A.sp杂化轨道形成σ键、未杂化的两个2p轨道形成两个π键, 是一种无色剧毒气体,其分子结构和NH 相似,但P-H键键能比N-H键键